美国食品和药物管理局周五批准了一种备受期待的新药,旨在减缓轻度和早期阿尔茨海默病患者的认知能力下降。
FDA 批准该药物 Leqembi(也称为 lecanemab)的几天前,该监管机构在国会报告中因其对另一种阿尔茨海默病药物 Aduhelm 的批准而受到严厉批评。
尽管试验结果显示单克隆抗体治疗有脑肿胀和出血的风险,但它还是被批准了。
这两种药物都是通过加速程序获得批准的,该程序允许 FDA 快速批准用于医疗需求未得到满足的严重疾病的药物。
FDA 在一份声明中表示,Leqembi 和 Aduhelm 由卫材和美国百健(Biogen)联合开发,“代表着有效治疗阿尔茨海默病的持续斗争取得的重要进展”。
“阿尔茨海默病极大地削弱了患者的生活能力,并对他们所爱的人造成了毁灭性的影响,”FDA 药物评估和研究中心的比利·邓恩 (Billy Dunn) 在一份声明中说。
邓恩说,Leqembi 是“针对和影响阿尔茨海默氏症潜在疾病过程的最新疗法,而不仅仅是治疗疾病的症状。”
大约有 650 万美国人患有阿尔茨海默氏症,其特征是记忆力减退和精神敏锐度下降。
Leqembi 试验的初步数据于 9 月发布,发现它使阿尔茨海默氏症患者的认知能力下降速度减慢了 27%。
第三阶段试验涉及近 1,800 人,分为接受药物治疗的人和接受安慰剂治疗的人,历时 18 个月。
完整的试验数据发表在新英格兰医学杂志上,引起了人们对包括脑出血和肿胀在内的“不良反应”发生率的担忧。
结果显示,服用该药物的患者中有 17.3% 出现脑出血,而接受安慰剂的患者中有 9% 出现脑出血。
服用该药物的人中有 12.6% 的人出现脑肿胀,而安慰剂组中只有 1.7% 的人出现脑肿胀。
该药物试验的两组报告的死亡率大致相同。
每年 26,500 美元
在阿尔茨海默病中,tau 蛋白和淀粉样蛋白 β 两种关键蛋白质形成缠结和斑块,统称为聚集体,会导致脑细胞死亡并导致脑萎缩。
Leqembi 每两周静脉注射一次,通过靶向淀粉样蛋白起作用。
在该试验中,与安慰剂组相比,接受 Leqembi 治疗的患者脑淀粉样斑块显着减少,而安慰剂组的 β 淀粉样斑块没有减少。
百健(Biogen)和卫材(Eisai)此前将 Aduhelm 推向市场,但对其是否有效存在重大争议,其 2021 年的批准导致 FDA 的三名高层辞职。
美国国会的一项调查称,加速批准 Aduhelm 的过程“充满违规行为”,该机构和百健(Biogen)均受到批评。
国会报告称,总部位于马萨诸塞州剑桥的 Biogen 为 Aduhelm 设定了每年 56,000 美元的“不合理的高价”。
卫材表示,Leqembi 最初的定价为每年 26,500 美元,并估计从现在起三年内将有 100,000 名美国人接受这种药物。
阿尔茨海默氏症协会兼首席执行官 Joanne Pike 对 Leqembi 的批准表示欢迎,但表示担心它的高成本可能会使大多数美国人无法负担,特别是如果它不在政府的老年人健康保险计划 Medicare 的覆盖范围内.
“今天患有这种致命疾病的人没有时间等待奇迹药物或治愈方法,”派克在一份声明中说。
- 标签:
智能推荐
-

美国隐瞒火星生命?NASA为何隐瞒真相40年未曾揭露2023-08-22 导语:如今人们对于寰宇的探索还在不断,此中火星算是比较往往研究的所在,时时刻刻都有专业的设备在凝望着火星的动向,然而人们也极端感兴趣火星能否有生命生计,传闻美国N
-

美国承认正在研究外星人 人类是不是宇宙中唯一的高等生物2023-08-10 没有确凿的证据证明这说法。长期以来,有关地外文明的存在与否一直是一个备受争议的话题。我们知道,在一个天体上产生生物并发展出文明是一个漫长而复杂的过程
-

同位素(同位素治疗疤痕多少钱)2023-09-07 同位素杂志社讲解刊名:同位素JournalofIsotopes主理:中国核学会同位素学会周期:季刊出书地:北京市语种:中文;开本:大16开ISSN:1-7512C
-
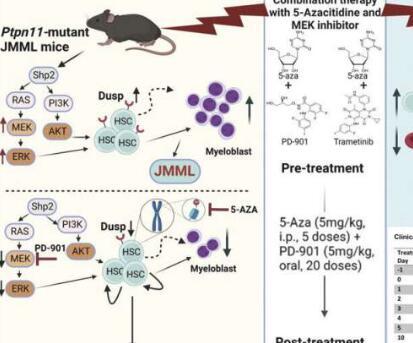
研究人员发现了治疗罕见儿科癌症的新药组合 称为JMML2023-08-28 印第安纳大学医学院的研究人员已经确定了一种有前途的新药物组合来治疗青少年粒单核细胞白血病(JMML),这是一种影响儿童的罕见血癌
-

荨麻疹到底怎么治(治疗荨麻疹的方法)2023-08-25 大家好,小范来为大家解答以上的问题。荨麻疹到底怎么治,治疗荨麻疹的方法这个很多人还不知道,现在让我们一起来看看吧
-

失眠是什么引起的怎么治疗(失眠是什么引起的)2023-09-07 大家好,小范来为大家解答以上的问题。失眠是什么引起的怎么治疗,失眠是什么引起的这个很多人还不知道,现在让我们一起来看看吧
-

世界上头发最长的人 来自美国的曼德拉(长发女人)2023-09-07 来自美国的女人曼德拉头发来到了17m。很多女人的头发都是比较长的,不过大部分女生也不过是刚刚到了肩的位置,哪怕再长一点也不过是到了腰的位置,如果比这个长度长很多,
-

美国小伙用10000个硬币铺地板,看到成品后,简直舍不得下脚!2023-08-31 随着时代的进步,高楼大厦在我们生活中已经见多不怪了,而且对于房子的装修,也是有各种各样的风格,在美国有一位小伙在装修新房的时候,觉得没有什么创意,后来突发奇想想用
-

血液稀释剂的受控局部输送可以改善血栓治疗2023-08-03 长期以来,肝素一直被用作血液稀释剂或抗凝剂,用于凝血障碍患者或手术后预防并发症。但药物仍然难以正确剂量,可能导致剂量过量或剂量不足
-

体重减轻可能是唐氏综合征患者阿尔茨海默病的早期预测指标2023-08-04 唐氏综合症患者的意外体重减轻可能早在记忆丧失和痴呆等典型认知症状明显之前就预测阿尔茨海默病的发作。多达9%的唐氏综合症患者在65岁时会出现阿尔茨海默氏症症状,但与
-
在美国119表示什么-竖中指在美国表示什么2023-09-12 美国火警电话号码是什么美国火警电话号码是911。美国通用的报警电话号码。消防电话、急救电话、报警电话都是911
-

绘制脑干对饮食的控制图可能会导致更好的肥胖治疗2023-08-25 你坐下来的每一顿饭都会给人留下深刻的印象,食物被当作美味的东西再次寻找,或者如果我们把这种味道与肠道不适联系起来,俗称胃痛,就会厌恶地避免
