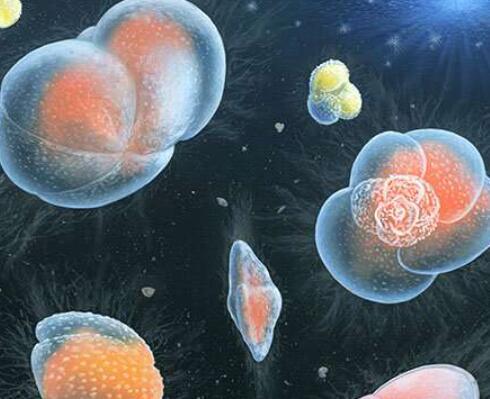
肿瘤抑制蛋白p53被称为“基因组的守护者”,通过触发细胞进行修复或自毁来保护身体的DNA免受日常压力或长期损伤。但是编码蛋白质的p53基因突变会阻止它执行其工作,使错误在遗传密码中积累并导致癌症等疾病。
宾夕法尼亚州立大学领导的一个研究小组首次使用患者样本发现了p53蛋白的完整结构。他们还研究了突变诱导的p53结构变化如何影响不同的癌症。他们在ChemBioChem和国际分子科学杂志上发表了他们的研究结果。
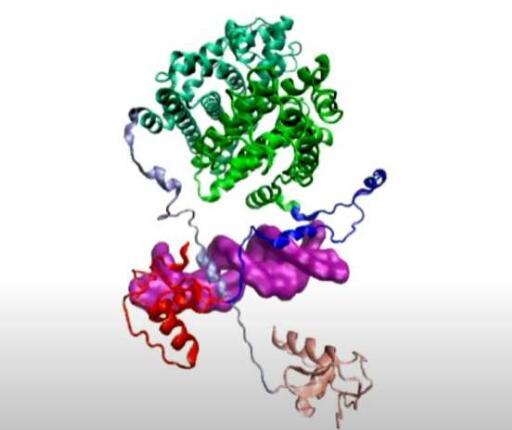
“我们定义了p53的全长结构,为理解可用于为新疗法提供信息的3D排列打开了大门,”宾夕法尼亚州立大学哈克生命科学研究所分子,细胞和综合生物科学博士生Maria Solares说。“科学家们此前已经将p53确定为肿瘤起源的重要焦点,并且已经对其在细胞中的功能进行了大量研究。然而,如果不了解p53的完整结构,我们对如何在患病细胞中处理它的知识是不完整的。
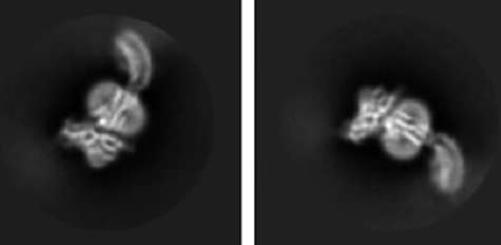
研究人员使用冷冻电子显微镜(cryo-EM)对从脑肿瘤细胞中分离的单个p53蛋白进行成像。Solares说,他们的工作独特之处在于,该团队使用半导体材料在成像之前干净地捕获分离的p53蛋白。这些基于硅的微芯片以这样一种方式保存蛋白质,研究人员可以解决以前看不见的分子特征。
“看到p53的完整结构就像在只观察有限的部分或四肢这么长时间后终于看到整个人体,”通讯作者Deb Kelly说,宾夕法尼亚州立大学生物医学工程教授,宾夕法尼亚州立大学结构肿瘤学中心主任和分子生物物理学哈克。“如果不了解他们的整个身体构成,就很难理解事物是如何运作的。
p53蛋白由称为单体的单个单元组成,它们结合形成更大的实体,或二聚体和四聚体。
“我们发现癌细胞内存在单体,二聚体和四聚体的混合物,每种化合物都根据细胞核内发生的事件服务于不同的目的,”Solares说。“二聚体结构的结果首次揭示了分子的'封闭'构型。这种形式的p53就像在比赛前处于起跑线上,当其他细胞信号通知存在问题时,准备好并准备向DNA跑去。
其他形式的p53,如单体,被认为是“开放的”,因为它们需要与另一个单元结合,然后才能移动到起跑线执行任务。根据凯利的说法,适当的沟通对于控制p53部署到DNA所在的细胞核的程度和时间非常重要,并且该过程的中断与包括癌症在内的疾病的起源有关。
p53基因的突变可能导致p53蛋白无法很好地沟通,凯利说。一旦他们揭示了3D结构,研究人员就研究了p53的结构变化如何导致分子在细胞内运作不正常。
“众所周知,一半的癌症都含有p53基因突变,”Solares说。“为了仔细研究这些突变如何影响p53蛋白结构,我们使用分子建模软件来模拟p53单体结构的变化。
研究人员研究了七个“热点”,其中蛋白质结构的突变最常与癌症有关。Kelly说,p53蛋白中的这七个突变通常会导致疾病进展和化学耐药性方面不利的患者预后。
他们发现突变p3的53D结构的轻微变化会影响蛋白质的表面电荷,从而排斥和吸引其他分子单位的电荷。根据凯利的说法,这会阻碍蛋白质和DNA之间的适当相互作用,导致p53协助维持健康细胞所必需的调节或修复过程的能力崩溃。
“在健康条件下,p53使用锌离子来紧密地保持遗传物质,”Solares说。“当蛋白质的表面电荷保持适当平衡时,锌离子可以占据正确的位置,以帮助p53抓住DNA。但是当p53基因的突变导致蛋白质表面的变化时,锌离子没有正确放置,p53失去了对DNA的控制。这种影响在疾病中进一步加剧。
研究人员表示,在未来,他们希望扩大他们的工作范围,研究p53突变密切相关的胰腺癌和卵巢癌。他们还在研究基于他们对p53全3D结构的新理解的新治疗方法。
“一个病人的癌症与另一个病人的癌症不一样,”索拉雷斯说。“我们需要不断收集来自不同患者和不同癌症的实验数据来测试我们的模型。没有完整的情况,我们就无法完全了解癌症。
除了Solares和Kelly之外,ChemBioChem论文的共同作者还包括来自宾夕法尼亚州立大学结构肿瘤中心的G. M. Jonaid,William Y. Luqiu,Samantha Berry,Janki Khadela,Madison C. Evans和William J. Dearnaley;以及来自弗吉尼亚理工大学弗拉林生物医学研究所的Yanping Liang,Zhi Sheng和Kevin J. Pirdham。
智能推荐
-

研究人员揭示了最古老的棘龙大脑2023-08-04 南安普敦大学和俄亥俄大学的研究人员重建了两只英国棘龙的大脑和内耳,帮助揭示了这些大型掠食性恐龙如何与环境相互作用
-

NBA75大球星官方完整名单(nba球星名单大全)2023-09-07 导语:近期NBA在75周年之际,分了三批告示出NBA75位闻名球形的名单,是由43名传奇球员、45位教授和总经理以及球队总管,共88人的评委团评比而成,因是凭据评
-

研究人员将植物蛋白机制转化为细菌 以帮助推进50年的努力2023-07-30 澳大利亚国立大学(ANU)的一个研究小组通过添加植物叶绿体中的多种成分来改变细菌的蛋白质折叠特性。这一成就使研究人员能够更详细地研究叶绿体蛋白,并找到更快地增强其
-
大规模化石研究揭示了15万年前现代生物多样性梯度的起源2023-08-10 研究人员已经使用了近五十万块化石来解决了一个2年的科学谜团:为什么不同物种的数量在赤道附近最多,并且向极地地区稳步减少
-

诀别诗胡彦斌完整版现场(诀别诗卓文君)2023-07-30 大家好,小范来为大家解答以上的问题。诀别诗胡彦斌完整版现场,诀别诗卓文君这个很多人还不知道,现在让我们一起来看看吧
-

旁的字形结构(旁边的旁是什么结构的字)2023-07-24 大家好,小裕来为大家解答以上问题。旁的字形结构,旁边的旁是什么结构的字这个很多人还不清楚,现在一起跟着小编来瞧瞧吧
-

动物为什么会进入冬眠:应对不利环境的自我保护(求生存)2023-08-20 我们都知道,近似蛇啊、松鼠啊、马来熊等动物都会进行蛰伏,并且蛰伏一进行即是数月,有的蛰伏时间更长的动物,一年中有9个月都在蛰伏
-

古代DNA分析揭示了米诺斯克里特岛的婚姻规则2023-07-20 来自德国莱比锡马克斯普朗克进化人类学研究所的一个国际研究小组报告了对希腊青铜时代婚姻规则和家庭结构的全新见解
-
研究人员揭示了对乳腺癌至关重要的蛋白质背后的动态2023-08-06 根据莱斯大学的科学家的说法,观看木偶戏可以教你一些关于雌激素如何在体内起作用的知识,他们的研究可以为调节激素的新策略打开大门-这可能有助于预防乳腺癌和其他疾病
-

年迈的父亲完整版(年迈的意思)2023-08-11 大家好,小范来为大家解答以上的问题。年迈的父亲完整版,年迈的意思这个很多人还不知道,现在让我们一起来看看吧
-
研究人员揭示了不寻常激素受体的结构2023-08-25 俗话说,养育一个孩子需要一个村庄。也需要一个村庄才能在科学和医学上取得进展。在这种情况下,来自哈佛医学院布拉瓦特尼克研究所的实验室,而不是两个,而是三个部门,以及
-

通过研究蜥蜴 研究人员揭示了塑造生物多样性的力量2023-08-12 “如果你在热带雨林中选择一个地方,计算15米内不同种类的蜥蜴的数量,你会得出一个数字,”卢克·马勒问道,“是什么
